Как уравнять коэффициенты в химическом уравнении. Карточка-информатор. "Алгоритм расстановки коэффициентов в уравнениях химических реакций."
В уроке 13 «» из курса «Химия для чайников » рассмотрим для чего нужны химические уравнения; научимся уравнивать химические реакции, путем правильной расстановки коэффициентов. Данный урок потребует от вас знания химических основ из прошлых уроков. Обязательно прочитайте об элементном анализе, где подробно рассмотрены эмпирические формулы и анализ химических веществ.
В результате реакции горения метана CH 4 в кислороде O 2 образуются диоксид углерода CO 2 и вода H 2 O. Эта реакция может быть описана химическим уравнением :
- CH 4 + O 2 → CO 2 + H 2 O (1)
Попробуем извлечь из химического уравнения больше сведений, чем просто указание продуктов и реагентов реакции. Химичекое уравнение (1) является НЕполным и потому не дает никаких сведений о том, сколько молекул O 2 расходуется в расчете на 1 молекулу CH 4 и сколько молекул CO 2 и H2 O получается в результате. Но если записать перед соответствующими молекулярными формулами численные коэффициенты, которые укажут сколько молекул каждого сорта принимает участие в реакции, то мы получим полное химическое уравнение реакции.
Для того, чтобы завершить составление химического уравнения (1), нужно помнить одно простое правило: в левой и правой частях уравнения должно присутствовать одинаковое число атомов каждого сорта, поскольку в ходе химической реакции не возникает новых атомов и не происходит уничтожение имевшихся. Данное правило основывается на законе сохранения массы, который мы рассмотрели в начале главы.
Нужно для того, чтобы из простого химического уравнения получить полное. Итак, перейдем к непосредственному уравниванию реакции (1): еще раз взгляните на химическое уравнение, в точности на атомы и молекулы в правой и левой части. Нетрудно заметить, что в реакции участвуют атомы трех сортов: углерод C, водород H и кислород O. Давайте подсчитаем и сравним количество атомов каждого сорта в правой и левой части химического уравнения.
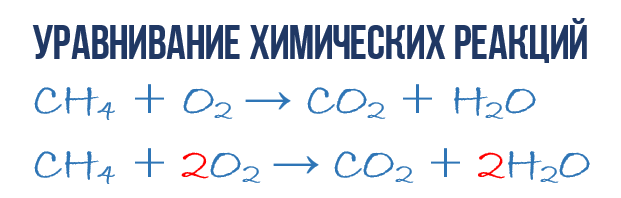
Начнем с углерода. В левой части один атом С входит в состав молекулы CH 4 , а в правой части один атом С входит в состав CO 2 . Таким образом в левой и в правой части количество атомов углерода совпадает, поэтому его мы оставляем в покое. Но для наглядности поставим коэффициент 1 перед молекулами с углеродом, хоть это и не обязательно:
- 1CH 4 + O 2 → 1CO 2 + H 2 O (2)
Затем переходим к подсчету атомов водорода H. В левой части присутствуют 4 атома H (в количественном смысле H 4 = 4H) в составе молекулы CH 4 , а в правой – всего 2 атома H в составе молекулы H 2 O, что в два раза меньше чем в левой части химического уравнения (2). Будем уравнивать! Для этого поставим коэффициент 2 перед молекулой H 2 O. Вот теперь у нас и в реагентах и в продуктах будет по 4 молекулы водорода H:
- 1CH 4 + O 2 → 1CO 2 + 2H 2 O (3)
Обратите свое внимание, что коэффициент 2, который мы записали перед молекулой воды H 2 O для уравнивания водорода H, увеличивает в 2 раза все атомы, входящие в ее состав, т.е 2H 2 O означает 4H и 2O. Ладно, с этим вроде бы разобрались, осталось подсчитать и сравнить количество атомов кислорода O в химическом уравнении (3). Сразу бросается в глаза, что в левой части атомов O ровно в 2 раза меньше чем в правой. Теперь-то вы уже и сами умеете уравнивать химические уравнения, поэтому сразу запишу финальный результат:
- 1CH 4 + 2O 2 → 1CO 2 + 2H 2 O или СH 4 + 2O 2 → CO 2 + 2H 2 O (4)
Как видите, уравнивание химических реакций не такая уж и мудреная штука, и важна здесь не химия, а математика. Уравнение (4) называется полным уравнением химической реакции, потому что в нем соблюдается закон сохранения массы, т.е. число атомов каждого сорта, вступающих в реакцию, точно совпадает с числом атомов данного сорта по завершении реакции. В каждой части этого полного химического уравнения содержится по 1 атому углерода, по 4 атома водорода и по 4 атома кислорода. Однако стоит понимать пару важных моментов: химическая реакция — это сложная последовательность отдельных промежуточных стадий, и потому нельзя к примеру истолковывать уравнение (4) в том смысле, что 1 молекула метана должна одновременно столкнуться с 2 молекулами кислорода. Процессы происходящие при образовании продуктов реакции гораздо сложнее. Второй момент: полное уравнение реакции ничего не говорит нам о ее молекулярном механизме, т.е о последовательности событий, которые происходят на молекулярном уровне при ее протекании.
Коэффициенты в уравнениях химических реакций
Еще один наглядный пример того, как правильно расставить коэффициенты в уравнениях химических реакций: Тринитротолуол (ТНТ) C 7 H 5 N 3 O 6 энергично соединяется с кислородом, образуя H 2 O, CO 2 и N 2 . Запишем уравнение реакции, которое будем уравнивать:
- C 7 H 5 N 3 O 6 + O 2 → CO 2 + H 2 O + N 2 (5)
Проще составлять полное уравнение, исходя из двух молекул ТНТ, так как в левой части содержится нечетное число атомов водорода и азота, а в правой — четное:
- 2C 7 H 5 N 3 O 6 + O 2 → CO 2 + H 2 O + N 2 (6)
Тогда ясно, что 14 атомов углерода, 10 атомов водорода и 6 атомов азота должны превратиться в 14 молекул диоксида углерода, 5 молекул воды и 3 молекулы азота:
- 2C 7 H 5 N 3 O 6 + O 2 → 14CO 2 + 5H 2 O + 3N 2 (7)
Теперь в обеих частях содержится одинаковое число всех атомов, кроме кислорода. Из 33 атомов кислорода, имеющихся в правой части уравнения, 12 поставляются двумя исходными молекулами ТНТ, а остальные 21 должны быть поставлены 10,5 молекулами O 2 . Таким образом полное химическое уравнение будет иметь вид:
- 2C 7 H 5 N 3 O 6 + 10,5O 2 → 14CO 2 + 5H 2 O + 3N 2 (8)
Можно умножить обе части на 2 и избавиться от нецелочисленного коэффициента 10,5:
- 4C 7 H 5 N 3 O 6 + 21O 2 → 28CO 2 + 10H 2 O + 6N 2 (9)
Но этого можно и не делать, поскольку все коэффициенты уравнения не обязательно должны быть целочисленными. Правильнее даже составить уравнение, исходя из одной молекулы ТНТ:
- C 7 H 5 N 3 O 6 + 5,25O 2 → 7CO 2 + 2,5H 2 O + 1,5N 2 (10)
Полное химическое уравнение (9) несет в себе много информации. Прежде всего оно указывает исходные вещества — реагенты , а также продукты реакции. Кроме того, оно показывает, что в ходе реакции индивидуально сохраняются все атомы каждого сорта. Если умножить обе части уравнения (9) на число Авогадро N A =6,022·10 23 , мы сможем утверждать, что 4 моля ТНТ реагируют с 21 молями O 2 с образованием 28 молей CO 2 , 10 молей H 2 O и 6 молей N 2 .
Есть еще одна фишка. При помощи таблицы Менделеева определяем молекулярные массы всех этих веществ:
- C 7 H 5 N 3 O 6 = 227,13 г/моль
- O2 = 31,999 г/моль
- CO2 = 44,010 г/моль
- H2 O = 18,015 г/моль
- N2 = 28,013 г/моль
Теперь уравнение 9 укажет еще, что 4·227,13 г = 908,52 г ТНТ требуют для осуществления полной реакции 21·31,999 г = 671,98 г кислорода и в результате образуется 28·44,010 г = 1232,3 г CO 2 , 10·18,015 г = 180,15 г H 2 O и 6·28,013 г = 168,08 г N 2 . Проверим, выполняется ли в этой реакции закон сохранения массы:
| Реагенты | Продукты | |
| 908,52 г ТНТ | 1232,3 г CO2 | |
| 671,98 г CO2 | 180,15 г H2 O | |
| 168,08 г N2 | ||
| Итого | 1580,5 г | 1580,5 г |
Но необязательно в химической реакции должны участвовать индивидуальные молекулы. Например, реакция известняка CaCO3 и соляной кислоты HCl, с образованием водного раствора хлорида кальция CaCl2 и диоксида углерода CO2 :
- CaCO 3 + 2HCl → CaCl 2 + CO 2 + H 2 O (11)
Химическое уравнение (11) описывает реакцию карбоната кальция CaCO 3 (известняка) и хлористоводородной кислоты HCl с образованием водного раствора хлорида кальция CaCl 2 и диоксида углерода CO 2 . Это уравнение полное, так как число атомов каждого сорта в его левой и правой частях одинаково.
Смысл этого уравнения на макроскопическом (молярном) уровне таков: 1 моль или 100,09 г CaCO 3 требует для осуществления полной реакции 2 моля или 72,92 г HCl, в результате чего получается по 1 молю CaCl 2 (110,99 г/моль), CO 2 (44,01 г/моль) и H 2 O (18,02 г/моль). По этим численным данным нетрудно убедиться, что в данной реакции выполняется закон сохранения массы.
Интерпретация уравнения (11) на микроскопическом (молекулярном) уровне не столь очевидна, поскольку карбонат кальция представляет собой соль, а не молекулярное соединение, а потому нельзя понимать химическое уравнение (11) в том смысле, что 1 молекула карбоната кальция CaCO 3 реагирует с 2 молекулами HCl. Тем более молекула HCl в растворе вообще диссоциирует (распадается) на ионы H + и Cl — . Таким образом более правильным описанием того, что происходит в этой реакции на молекулярном уровне, дает уравнение:
- CaCO 3 (тв.) + 2H + (водн.) → Ca 2+ (водн.) + CO 2 (г.) + H 2 O(ж.) (12)
Здесь в скобках сокращенно указано физическое состояние каждого сорта частиц (тв. — твердое, водн. — гидратированный ион в водном растворе, г. — газ, ж. — жидкость).
Уравнение (12) показывает, что твердый CaCO 3 реагирует с двумя гидратированными ионами H + , образуя при этом положительный ион Ca 2+ , CO 2 и H 2 O. Уравнение (12) как и другие полные химические уравнения не дает представления о молекулярном механизме реакции и менее удобно для подсчета количества веществ, однако, оно дает лучшее описание происходящего на микроскопическом уровне.
Закрепите полученные знания о составлении химических уравнений, самостоятельно разобрав пример с решением:
Надеюсь из урока 13 «Составление химических уравнений » вы узнали для себя что-то новое. Если у вас возникли вопросы, пишите их в комментарии.
Преподаватель, являясь главным действующим лицом в организации познавательной деятельности учащихся, постоянно находится в поиске путей повышения эффективности обучения. Организация эффективного обучения возможна только при знании и умелом использовании разнообразных форм педагогического процесса.
1. Современный человек должен обладать, не только суммой знаний и умений, но и способностью воспринимать мир как единое, сложное, постоянно развивающееся целое.
Скачать:
Предварительный просмотр:
Статья по химии: «Расстановка коэффициентов в химических уравнениях»
Составила: учитель химии
ГБОУ СОШ № 626
Казутина О.П.
Москва 2012
«Расстановка коэффициентов в химических уравнениях»
Преподаватель, являясь главным действующим лицом в организации познавательной деятельности учащихся, постоянно находится в поиске путей повышения эффективности обучения. Организация эффективного обучения возможна только при знании и умелом использовании разнообразных форм педагогического процесса.
1. Современный человек должен обладать, не только суммой знаний и умений, но и способностью воспринимать мир как единое, сложное, постоянно развивающееся целое.
Алгоритм работы по подготовке к проведению урока
выбор темы, определение целеполагания;
отбор содержания;
определение средств и путей развития у учащихся положительной мотивационной установки к работе на уроке;
конкретизация оснащения урока необходимым наглядным и дидактическим материалом;
разработка конспекта урока
Пример урока химии «Расстановка коэффициентов в химическом уравнении» для учителей
Цель: ответить на вопрос: «для чего надо расставлять коэффициенты в химическом уравнении»
Задачи:
Проблема необходимости расстановки коэффициентов
Алгоритм расстановки коэффициентов
Доказательство смысла расстановки коэффициентов
Ход урока:
Современный ученик, если он и учится, то относится к получаемым и перерабатываемым знаниям с прагматичностью. Поэтому предоставляемый материал должен уложиться в голове логично и лаконично.
Чтобы этого добиться, учителю всегда следует обращать внимание на то, зачем надо усвоить на уроке то или иное действие. То есть учитель должен объяснить. А потом, по – хорошему, дождаться правильных вопросов по новой теме.
Закон сохранения массы веществ
Знаменитый английский химик Р. Бойль, прокаливая в открытой реторте различные металлы и взвешивания их до и после нагревания, обнаружил, что масса металлов становится больше. Основываясь на этих опытах, он не учитывал роль воздуха и сделал неправильный вывод, что масса веществ в результате химических реакций изменяется. Р. Бойль утверждал, что существует какая-то "огненная материя", которая в случае нагревания металла соединяется с металлом, увеличивая массу.
Mg + O 2 MgO
24 г
40 г
М. В. Ломоносов в отличие от Р. Бойля прокаливал металлы не на открытом воздухе, а в запаянных ретортах и взвешивал их до и после прокаливания. Он доказал, что масса веществ до и после реакции остается без изменения и что при прокаливании к металлу присоединяется какая-то часть воздуха. (Кислород в то время не был еще открыт.) Результаты этих опытов он сформулировал в виде закона: "Все перемены,в натуре случающиеся, такого суть состояния, что сколько чего у одного тела отнимается столько присовокупится к другому". В настоящее время этот закон формулируется так:
Масса веществ, вступивших в химическую реакцию, равна массе образовавшихся веществ
Mg + O 2 MgO
24 г 32 г 40 г
Вопрос: закон не выполняется (т.к. не равны массы исходных и конечных веществ).
Решение этой проблемы – расстановка коэффициентов (целых чисел, показывающих количество молекул):
2Mg + O 2 2MgO
48 г 32 г 80 г – массы до и после равны благодаря тому, что число атомов элементов тоже равно до и после реакции.
Таким образом, доказав учащимся необходимость уравнивания масс коэффициентов, можно даже обойтись без некоторых предыдущих тем: составления формул веществ по валентности, расчета массы, количество вещества…Также рассказ о том, что закон сохранения массы вещества 20 лет спустя «переоткрыл» А. Лавуазье, уточнив его с одной стороны, но совершенно не обратив внимания на М.В. Ломоносова с этической, можно оставить на самостоятельное изучение в виде доклада, например.
Итак, для успешного выполнения заданий такого рода, необходимо усвоить условие: число атомов до реакции дб равно числу атомов после реакции: решим вместе:
H 2 S + 3O 2 SO 2 + 2H 2 O (удваиваем кислороды справа. Считаем их слева)
СН 4 + 2О 2 СО 2 + 2Н 2 О
Мы расставили коэффициенты в уравнениях горения двух газов
Сегодня мы поговорим о том, как расставлять коэффициенты в химических уравнениях. Данный вопрос интересует не только старшеклассников общеобразовательных учреждений, но и ребят, которые только знакомятся с основными элементами сложной и интересной науки. Если на первом этапе понять, в будущем проблем с решением задач не появится. Давайте разбираться с самого начала.
Что такое уравнение
Под ним принято подразумевать условную запись химической реакции, протекающей между выбранными реагентами. Для такого процесса используют индексы, коэффициенты, формулы.
Алгоритм составления
Как оформить химические уравнения? Примеры любых взаимодействий можно написать, суммируя исходные соединения. Знак равенства свидетельствует о том, что между реагирующими веществами протекает взаимодействие. Далее составляется формула продуктов по валентности (степени окисления).
Как записать реакцию
Например, если нужно записать химические уравнения, подтверждающие свойства метана, выбираем следующие варианты:
- галогенирование (радикальное взаимодействие с элементом VIIA периодической таблицы Д. И. Менделеева);
- горение в кислороде воздуха.
Для первого случая в левой части пишем исходные вещества, в правой - полученные продукты. После проверки числа атомов каждого химического элемента получаем конечную запись происходящего процесса. При горении метана в кислороде воздуха происходит экзотермический процесс, в результате которого образуется углекислый газ и водяной пар.
Для того чтобы правильно поставить коэффициенты в химических уравнениях, используется закон сохранения массы веществ. Начинаем процесс уравнивания с определения количества атомов углерода. Далее проводим расчеты для водорода и только после этого проверяем количество кислорода.
ОВР
Сложные химические уравнения можно уравнять, вооружившись методом электронного баланса или полуреакций. Предлагаем последовательность действий, предназначенную для расстановки коэффициентов в реакциях следующих типов:
- разложения;
- замещения.

Сначала важно расставить у каждого элемента в соединении степени окисления. При их расстановке необходимо учитывать некоторые правила:
- У простого вещества она равна нулю.
- В бинарном соединении их сумма равна 0.
- В соединении из трех и более элементов у первого проявляется положительная величина, у крайнего иона - отрицательное значение степени окисления. Центральный элемент высчитывают математическим путем, учитывая, что в сумме должен быть 0.
Далее выбирают те атомы либо ионы, у которых изменился показатель степени окисления. Знаками «плюс» и «минус» показывают количество электронов (принятых, отданных). Далее между ними определяется наименьшее кратное. При делении НОК на эти цифры получают числа. Данный алгоритм и будет ответом на вопрос о том, как расставлять коэффициенты в химических уравнениях.
Первый пример
Допустим, дано задание: «Расставьте коэффициенты в реакции, дополните пропуски, определите окислитель и восстановитель». Такие примеры предлагаются выпускникам школы, которые выбрали химию в качестве ЕГЭ.
KMnO 4 + H 2 SO 4 + KBr = MnSO 4 + Br 2 +…+…

Попробуем понять, как расставлять коэффициенты в химических уравнениях, предлагаемых будущим инженерам и медикам. После расстановки степеней окисления у элементов в исходных веществах и имеющихся продуктах получаем, что в качестве окислителя выступает ион марганца, а восстановительные свойства демонстрирует бромид-ион.
Делаем вывод о том, что пропущенные вещества не участвуют в окислительно-восстановительном процессе. Одним из недостающих продуктов является вода, а вторым станет сульфат калия. После составления электронного баланса завершающим этапом станет постановка коэффициентов в уравнении.
Второй пример
Приведем еще один пример, чтобы понять, как расставлять коэффициенты в химических уравнениях окислительно-восстановительного вида.
Допустим, дана следующая схема:
P + HNO 3 = NO 2 + … + …
Фосфор, который по условию является простым веществом, проявляет восстановительные свойства, повышая степень окисления до +5. Поэтому одним из пропущенных веществ будет фосфорная кислота H 3 PO 4. ОВР предполагает наличие восстановителя, которым будет выступать азот. Он переходит в оксид азота (4), образуя NO 2

Для того чтобы поставить в этой реакции коэффициенты, составим электронный баланс.
P 0 отдает 5e = P +5
N +5 принимает e = N +4
Учитывая, что перед азотной кислотой и оксидом азота (4) должен стоять коэффициент 5, получаем готовую реакцию:
P + 5HNO 3 =5NO 2 + H 2 O + H 3 PO 4
Стереохимические коэффициенты в химии позволяют решать разнообразные расчетные задачи.
Третий пример
Учитывая, что расстановка коэффициентов вызывает у многих старшеклассников затруднения, необходимо отрабатывать последовательность действий на конкретных примерах. Предлагаем еще один пример задания, выполнение которого предполагает владение методикой расстановки коэффициентов в окислительно-восстановительной реакции.
H 2 S + HMnO 4 = S + MnO 2 +…

Особенность предложенного задания в том, что необходимо дополнить пропущенный продукт реакции и только после этого можно переходить к постановке коэффициентов.
После расстановки степеней окисления у каждого элемента в соединениях можно сделать вывод, что окислительные свойства проявляет марганец, понижающий валентность. Восстановительную способность в предложенной реакции демонстрирует сера, восстанавливаясь до простого вещества. После составления электронного баланса нам останется только расставить коэффициенты в предлагаемую схему процесса. И дело сделано.
Четвертый пример
Химическое уравнение называют полным процессом в том случае, когда в нем в полном объеме соблюдается закон сохранения массы веществ. Как проверить эту закономерность? Количество атомов одного вида, которые вступили в реакцию, должно соответствовать их числу в продуктах взаимодействия. Только в этом случае можно будет вести речь о полноценности записанного химического взаимодействия, возможности его применения для проведения вычислений, решения расчетных задач разного уровня сложности. Приведем вариант задания, предполагающего расстановку в реакции недостающих стереохимических коэффициентов:
Si + …+ HF = H 2 SiF 6 + NO +…

Сложность задания в том, что пропущены и исходные вещества, и продукты взаимодействия. После постановки всех элементов степеней окисления видим, что восстановительные свойства проявляет в предлагаемом задании атом кремния. Среди продуктов реакции присутствует азот (II), одним из исходных соединений является азотная кислота. Логическим путем определяем, что недостающим продуктом реакции является вода. Завершающим этапом будет расстановка полученных стереохимических коэффициентов в реакцию.
3Si + 4HNO 3 + 18HF = 3H 2 SiF 6 + 4NO + 8 H 2 O
Пример задачи на уравнение
Нужно определить объем 10 % раствора хлороводорода, плотность которого составляет 1,05 г/мл, необходимый для полной нейтрализации гидроксида кальция, образующегося в процессе гидролиза его карбида. Известно, что газ, выделяющийся в ходе гидролиза, занимает объем 8,96 л (н. у.) Для того чтобы справиться с поставленным заданием, необходимо сначала составить уравнение процесса гидролиза карбида кальция:
CaC 2 + 2H 2 O = Ca (OH) 2 + C 2 H 2
Гидроксид кальция вступает во взаимодействие с хлороводородом, происходит полная нейтрализация:
Ca (OH) 2 + 2HCl = CaCl 2 + 2H 2 O

Вычисляем массу кислоты, которая потребуется для данного процесса. Определяем объем раствора хлороводорода. Все расчеты по задаче проводятся с учетом стереохимических коэффициентов, что подтверждает их важность.
В заключение
Анализ результатов единого государственного экзамена по химии свидетельствует о том, что задания, связанные с постановкой стереохимических коэффициентов в уравнениях, составление электронного баланса, определение окислителя и восстановителя вызывают серьезные затруднения у современных выпускников общеобразовательных школ. К сожалению, степень самостоятельности современных выпускников практически минимальна, поэтому отработку теоретической базы, предложенной педагогом, старшеклассники не проводят.
Среди типичных ошибок, которые допускают школьники, расставляя коэффициенты в реакциях разного типа, много математических погрешностей. Например, не все умеют находить наименьшее общее кратное, правильно делить и умножать числа. Причина подобного явления в уменьшении количества часов, выделяемых в образовательных школах на изучение данной темы. При базовой программе по химии у педагогов нет возможности отрабатывать со своими школьниками вопросы, касающиеся составления электронного баланса в окислительно-восстановительном процессе.
Инструкция
Прежде чем приступать к самому заданию, нужно усвоить, что цифра, которая ставится перед химическим элементом или всей формулой коэффициентом. А цифра, стоящая (и чуть ) индекс. Кроме этого , что:
Коэффициент относится ко всем химическим символам, стоящим после него в формуле
Коэффициент умножается на индекс (не складывается!)
Атомов каждого элемента вступающих в реакцию веществ должно совпадать с числом атомов этих элементов, входящих в продуктов реакции.
Например, запись формулы 2H2SO4 означает 4 атома H (водорода), 2 атома S (серы) и 8 атомов O (кислорода).
1. Пример № 1. Рассмотрим горения этилена.
При сгорании органического вещества образуются оксид углерода (IV) (углекислый газ) и вода. Попробуем последовательно коэффициенты.
C2H4 + O2 => CO2+ H2O
Начинаем анализировать. В реакцию в ступило 2 атома С (углерода), а получился только 1 атом, значит перед CO2 ставим 2. Теперь их количество одинаково.
C2H4 + O2 => 2CO2+ H2O
Теперь смотрим на H (водород). В реакцию вступило 4 атома водорода, а получилось в результате только 2 атома, следовательно, перед H2O (водой) ставим 2 – теперь получилось тоже 4
C2H4 + O2 => 2CO2+ 2H2O
Считаем все атомы О (кислорода), образовавшиеся в результате реакции (то есть, после равенства). 4 атома в 2CO2 и 2 атома в 2H2O – всего 6 атомов. А до реакции всего 2 атома, значит, перед молекулой кислорода O2 ставим 3, а значит, их стало тоже 6.
C2H4 + 3O2 => 2CO2+ 2H2O
Таким образом, получилось одинаковое количество атомов каждого элемента до и после знака равенства.
C2H4 + 3O2 => 2CO2+ 2H2O
2. Пример № 2. Рассмотрим реакцию взаимодействия алюминия с разбавленной серной кислотой.
Al + H2SO4 => Al2 (SO4) 3 + H2
Смотрим на атомы S, входящие в состав Al2 (SO4) 3 - их 3, а в H2SO4 (серной кислоте) только 1, следовательно, и перед серной кислотой тоже ставим 3.
Al + 3H2SO4 => Al2 (SO4) 3 + H2
Зато теперь получилось до реакции 6 атомов H (водорода), а после реакции только 2, значит, перед молекулой H2 (водорода) ставим тоже 3, чтобы в целом получилось 6.
Al + 3H2SO4 => Al2 (SO4) 3 + 3H2
В последнюю очередь смотрим на . Так как в Al2 (SO4) 3 (сульфате алюминия) всего 2 атома алюминия, то и до реакции перед Al (алюминием) ставим 2.
2Al + 3H2SO4 => Al2 (SO4) 3 + 3H2
Теперь количество всех атомов до и после реакции совпадает. Оказалось, что расставлять коэффициенты в химических уравнениях не так и сложно. Достаточно потренироваться и все получится.
Обязательно учитывайте, что коэффициент умножается на индекс, а не складывается.
Источники:
- как элементы вступают в реакцию
- Тест по теме «Химические уравнения»
Для многих школьников написать уравнения химических реакций и правильно расставить коэффициенты нелегкая задача. Причем, главную трудность у них почему-то вызывает именно вторая ее часть. Казалось бы, ничего сложного в том нет, однако порой ученики пасуют, впадая в полную растерянность. А ведь надо всего лишь запомнить несколько простых правил, и задача перестанет вызывать затруднения.
Инструкция
Коэффициент, то есть число, стоящее перед формулой молекулы химического вещества, ко всем символам, и умножается на каждый каждого символа! Именно умножается, а не складывается! Это может показаться невероятным, но некоторые школьники складывают два числа вместо того, чтобы их перемножить.
Количество атомов каждого элемента исходных веществ (то есть находящихся в левой части уравнения) должно совпадать с количеством атомов каждого элемента продуктов реакции (соответственно, находящихся в его правой части).
Самое простое уравнение реакции:
Fe + S => FeS
Уравнение реакции нужно уметь не только записать, но и прочитать. Это уравнениев простейшем варианте читается так: молекула железа взаимодействует с молекулой серы, получается одна молекула сульфида железа.
Самое трудное в написании уравнения реакции- составить формулы продуктов реакции, т.е. образующихся веществ. Здесь правило только одно: формулы молекул строятся строго по валентности составляющих их элементов.
Кроме того, при составлении уравнений реакций надо помнить о законе сохранения массы веществ: все атомы молекул исходных веществ должны войти в состав молекул продуктов реакции. Ни один атом не должен исчезнуть или неожиданно появиться. Поэтому иногда, записав все формулы в уравнении реакции, приходится выравнивать число атомов в каждой части уравнения- расставлять коэффициенты. Вот пример:
С + O 2 => CO 2Здесь у каждого элемента одинаковое число атомов и в правой, и в левой части уравнения. Уравнение готово.
Cu + O 2 => CuO
А здесь атомов кислорода в левой части уравнения больше, чем в правой. Нужно, чтобы получилось столько молекул оксида меди
CuO , чтобы в них оказалось столько же атомов кислорода, т.е.2. Поэтому передформулой СuО ставим коэффициент2:Cu + O 2 => 2 CuO
Теперь неодинаково число атомов меди. В левой части уравнения перед знаком меди ставим коэффициент2:
2 Cu + O 2 => 2 CuO
Посчитайте, поровну ли атомов каждого элемента в левой и правой частях уравнения. Если да, то уравнение реакции составлено правильно.
Еще один пример: Al + O 2 = Al 2 O 3
И здесь атомов каждого элемента разное количество до реакции и после нее. Выравнивать начинаем с газа- с молекул кислорода:
1) Слева2 атома кислорода, а справа3. Ищем наименьшее общее кратное двух этих чисел. Это наименьшее число, которое делится и на2, и на3, т.е.6. Перед формулами кислорода и оксида алюминия Al 2 O 3 ставим такие коэффициенты, чтобы общее число атомов кислорода в этих молекулах было6:
Al + 3 O 2 = 2 Al 2 O 3
2) Считаем число атомов алюминия: слева1 атом, а справа в двух молекулах по2 атома, т.е.4. Перед знаком алюминия в левой части уравнения ставим коэффициент4:
4 Al + 3O 2 => 2 Al 2 O 3
3) Еще раз пересчитываем все атомы до реакции и после нее: по 4 атома алюминия и по 6 атомов кислорода.
Все в порядке, уравнение реакции составлено верно. А если реакция идет при нагревании, то над стрелкой дополнительно ставится знак t .
Уравнение химической реакции- это запись хода химической реакции с помощью химических формул и коэффициентов.

 Вход
Вход